Back to: QUÍMICA 4
Cuando hablamos de los elementos químicos de la tabla periódica, los podemos reconocer gracias a su símbolo. Sin embargo, cuando hablamos de compuestos tenemos que reconocer que estos, pueden tener dos o más combinaciones de elementos. Estos compuestos conforman la materia con la que comúnmente estamos en contacto. Sólo los elementos que son gases nobles se encuentran normalmente en la naturaleza como átomos aislados.
Los compuestos, poseen una fórmula química que se representa con la abreviatura de los elementos que lo conforman. Además poseen un número o subíndice que indica el número de átomos que participan para generar el compuesto, por ejemplo:
| NaCl | Participa un átomo de Na y uno de Cl para formar cloruro de sodio. |
| Na2S | Participan dos átomos de Na y uno de azufre para formar sulfuro de sodio. |
| CaF2 | Participa un átomo de calcio y dos de flúor para formar fluoruro de calcio. |
La capacidad combinatoria de los elementos que conforman un compuesto, depende de los números de oxidación de cada uno de ellos. Esto es muy importante ya que permite determinar el número de átomos (representados como subíndice en la fórmula química) que van a conformar una fórmula química.
Recordemos que los elementos en la tabla periódica se encuentran organizados por número atómico y, además podemos estudiarlos de acuerdo a sus propiedades físicas y químicas. Una gran proporción de los elementos en la tabla periódica son metales, los cuales pierden electrones para formar iones positivos (cationes). Mientras que, los no metales ganan electrones para formar iones negativos (aniones).
La nomenclatura química consiste en una serie de reglas específicas para cada tipo de compuestos, ya sean inorgánicos y orgánicos, que se emiten por una comisión de la IUPAC (Union International of Pure Applied Chemistry). La finalidad de la IUPAC es la de asignar un nombre a cada sustancia si se conoce su composición o una fórmula si lo que se conoce es el nombre.
De acuerdo al número de elementos diferentes que se combinan, los compuestos se dividen en:
| Binarios: Constituidos por la unión de dos elementos diferentes. | FeO, CuO, NaCl, N2O, H2O, NH3 |
| Ternarios: Constituidos por la combinación de tres elementos diferentes. | H2SO4, H2CO3, AgNO3, NaOH |
| Cuaternarios: Constituidos por la combinación de cuatro elementos diferentes. | NaHCO3, NaHSO4 |
También debemos considerar que, los elementos poseen números de oxidación característicos. Los números de oxidación son cargas que posee un átomo en una molécula (ó compuesto iónico) si contabilizáramos los electrones.
Para ello, existen reglas, que nos permiten asignar los números de oxidación a los elementos que participan en un compuesto:
- Los elementos libres o moleculares que no estén combinados con otro diferente presentan el número cero. Ejemplos: Cu, Fe, O2, N2, H2.
- En iones monoatómicos, el número de oxidación es igual a la carga en el ión. Por ejemplo, Na+ es +1, Cl– es -1, P3- es -3, Ca+2 es +2.
- El número de oxidación del oxígeno es generalmente 2-, excepto en peróxidos que es de 1-, como el peróxido de hidrógeno (H2O2).
- El número de oxidación del hidrógeno es 1+. Excepto cuando se enlaza a los metales y compuestos binarios, en estos casos, su número de oxidación es 1-, como el hidruro de sodio (NaH) ó el hidruro de calcio (CaH2).
- Los elementos del grupo IA, IIA y IIIA tienen carga de 1+, 2+, 3+ respectivamente. El flúor siempre es 1-.
- Todos los metales tienen un número de oxidación con carga positiva.
Podemos observar que, en la tabla periódica los elementos tienen números de oxidación característicos que les permiten reaccionar de manera específica para formar compuestos.
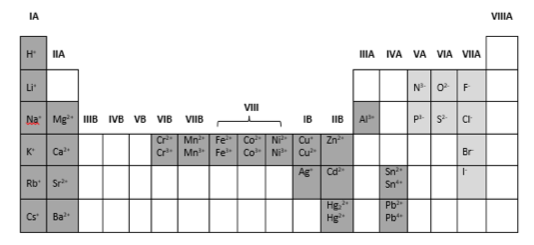
Relación periódica de iones sencillos comunes.
En las siguientes tablas podemos notar los principales cationes y aniones:


† Para los iones derivados del Yodo y el Bromo que se combinan con el Oxígeno, se nombran de la misma manera que el Cloro.
Con lo expuesto anteriormente, ahora podemos comenzar a dar nombre a los compuestos iónicos, así como a generar sus fórmulas correspondientes. Primero se nombra el anión seguido de la conjunción “de”, seguido del nombre del catión. Debemos notar que además, de que todos los compuestos son neutros; la carga global (suma de cargas positivas y negativas) de los compuestos es cero.
A continuación, se muestra algunos ejemplos de fórmulas y sus nombres. Es importante denotar como se mencionó anteriormente en la asignación de números de oxidación, que la suma de las cargas debe ser igual a cero, pero muchas veces se pueden combinar cationes y aniones con cargas distintas. Por lo que, se coloca un subíndice que indica el número de iones que se combinan para que la suma neta de las cargas sea igual a cero.
† Para los iones derivados del Yodo y el Bromo que se combinan con el Oxígeno, se nombran de la misma manera que el Cloro.
Con lo expuesto anteriormente, ahora podemos comenzar a dar nombre a los compuestos iónicos, así como a generar sus fórmulas correspondientes. Primero se nombra el anión seguido de la conjunción “de”, seguido del nombre del catión. Debemos notar que además, de que todos los compuestos son neutros; la carga global (suma de cargas positivas y negativas) de los compuestos es cero.
A continuación, se muestra algunos ejemplos de fórmulas y sus nombres. Es importante denotar como se mencionó anteriormente en la asignación de números de oxidación, que la suma de las cargas debe ser igual a cero, pero muchas veces se pueden combinar cationes y aniones con cargas distintas. Por lo que, se coloca un subíndice que indica el número de iones que se combinan para que la suma neta de las cargas sea igual a cero.


Además de los iones sencillos o monoatómicos, en las tablas de cationes y aniones, sobresalen iones poliatómicos que contienen más de un tipo de átomo. Por lo que, cuando se combinan con un respectivo ión de carga contraria estos se encierran con un paréntesis. Cuando está presente más de una unidad del ión, es decir, cuando se escribe la fórmula química de un compuesto que tiene un ión pliatómico, el ión se encierra entre paréntesis seguidos de un subíndice, que indica el número de iones poliatómicos presentes. Por ejemplo:

Ahora bien, una vez que ya reconocemos como se pueden escribir las fórmulas químicas y las reglas que siguen para la asignación de fórmulas químicas, es necesario reconocer cómo podemos combinarlos y el nombre de los compuestos que se generan.
Si seguimos el siguiente esquema podremos reconocer el tipo de compuesto que se genera si lo combinamos con oxígeno, hidrogeno o en ausencia de ambos.
